MEKANISME REAKSI OKSIDASI PADA BERABAGAI SENYAWA ORGANIK
MEKANISME REAKSI OKSIDASI PADA BERBAGAI SENYAWA ORGANIK
Oksidasi adalah reaksi yang mengalami peningkatan bilangan oksidasi dan penurunan elektron. Dimana reaksi oksidasi ini dapat dikatakan bahwa oksidasi adalah reaksi dimana suatu zat yang terikat dengan oksigen. Pada reaksi oksidasi ini, oksigen yang digunakan bukanlah oksigen yang bebas, melainkan dengan menggunakan oksigen yang pekat, yang berada dalam suasana asam dan lainnya.
Reaksi oksidasi memiliki karakterisktik pada senyawa organik, dapat ditinjau berdasarkan ikatan C-O nya yang hasilnya lebih banyak dan hasil dari ikatan C-H yang sedikit.
Terdapat bebagai macam jenis mekanisme reaksi oksidasi pada senyawa organik. Diantaranya adalah :
1. Oksidasi Bayer-Villiger
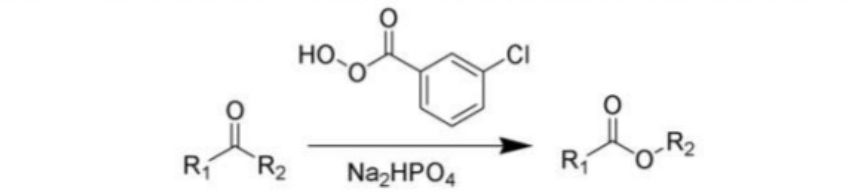
Oksidasi Bayer-Villiger adalah reaksi yang mengubah keton sehingga menjadi ester yang dirubah oleh oksidasi asam peroksi. Reaksi ini dapat berlangsung secara enzimatis ataupun kimia. Salah satu jenis bakteri yang bisa mengekspresikan suatu enzim sikloheksanon monooksigen yang termasuk suatu biokatalis pada reaksi oksidasi Beayer_Villiger yaitu isolat Pseudomonas sp. P5-LS 3/2. Bakteri ini merupakan isolat bakteri dari genus pseudomonas sp.
Reaksinya :
Mekanisme Reaksi :
2. Reaksi Oksidasi Pfitzer-Moffat
Reaksi oksidasi Pfitzer-Moffat adalah suatu cara oksidasi yang mana umumnya berperan penting dan dilakukan dengan menambahkan alkohol dan dicampurkan dengan larutan disikloheksil karbodimida (DCC) dan pridinium trifluoro asetat, dan kemudian ditambahkan dengan pelarut yang inert misalnya benzena atau 1,2-di-metoksi etana umtuk memberikan hasil yang baik.
Mekanisme Reaksi nya adalah:
3. Reaksi Oksidasi Jones
Reaksi oksidasi Jones ini merupakan suatu reaksi kimia yang menggambarkan oksidasi asam kromat untuk mengoksidasi aldehid ataupun alkohiol. Asam kromat lebih cenderung untuk menyerang ikatan karbon sekunder.
Suatu reaksi alkohol dengan larutan asam kromat berair dalam aseton untuk membentuk ester kromat yang seimbang dan kemudian suatu senyawa Cr (IV) dieliminasi sehingga menghasilkan keton. Senyawa Cr (IV) ini diubah menjadi Cr(III) yang stabil melalui deretan reaksi cepat lainnya.
Mekanisme Reaksi :
Selain dari reaksi diatas, terdapat beberapa reaksi yang ada pada senyawa organik :
1. Reaksi Oksidasi Pada Alkena dengan KMnO4 Pekat
Pada reaksi ini alkena dengan KMnO4 terlibat dalam pemutusan ikatan C=C alkena. Reaksi ini hampir mirip dengan reaksi ozonolisis alkena. Hanya saja, dalam hal ini disebabkan KMnO4 merupakan oksidator yang kuta, sehingga aldehid yang terbentuk akan teroksidasi menjadi asam karboksilat.
Contoh reaksi nya:
Berdasarkan dari reaksi tersebut terdapat dua tahap yang terbentuk, yaitu :
Tahap 1 : Pembentukan Diol, dimana pada tahap ini alkena teroksidasi menjadi diol.
Tahap 2: Oksidasi Diol, yang mana pada tahp ini diol yang terbentuk pada tahap pertama akan teroksidasi lagi sehingga menghasilkan produk akhir yaitu asam karboksilat dan keton.
Oksidasi alkohol merupakan reaksi yang berperan penting dalam kimia organik. Karena adanya alkohol primer yang dapat dioksidasi sehingga membentuk aldehida dan asam karboksilat. Kemudian adanya alkohol sekunder yang dapat dioksidasi untuk menghasilkan keton dan terdapatnya alkohol tersier. Akan tetapi pada alkohol tersier ini merupakan kebalikan dari alkohol primer dan alkohol sekunder dimana pada alkohol tersier ini tidak dapat dioksidasi tanpa memutuskan ikatan pada molekul C-C.
Oksidasi primer dapat teroksidasi menjadi aldehida ataupun asam karboksilat, tetapi bergantung pada kondisi reaksinya. Pada saat proses terbentuknya asam karboksilat, pertama-tama alkohol teroksidasi menjadi aldehida dan kemudian dioksidasi lagi lebih lanjut sehingga menjadi asam.
Pada alkohol sekunder, dioksidasi menjadi keton. Misalnya, ketika kita memanaskan propanon -2-ol sekunder dengan larutan natrium atau kalium dikromat (VI) kemudian diasamkan dengan asam sulfat encer, dan didapatkan hasilnya yang terbentuk adalah propana.
Kemudian pada alkohol tersier yang tidak dapat dioksidasi dengan larutan natrium atau kalium dikromat 9VI) yang diasamkan sehingga tidak ada reaksi apapun. Jika dilihat hasil yang terjadi dengan alkohol primer dan sekunder, maka akan terlihat bahwa zat yang menjadi pengoksidasi akan mengeluarkan hidrogen dari gugus -OH kemudian hidrogen dari atom-atom karbon akan terikat pada -OH. Alkohol tersier tidak memiliki atom hidrogen yang terikat pada karbon itu.
3. Reaksi Oksidasi Pada Aldehid dan Keton
Oksidasi pada aldehida akan mudah terjadi jika terdapatnya atom hidrogen. Dengan kata lain, mereka merupakan agen pereduksi yang kuat. Pada reaksi ini, umumnya akan menghasilkan hasil yang baik jika berada pada suhu kamar.
Reaksi asam pada reaksi sebelumnya akan dapat menyebabkan reaksi samping yang tidak dapat diinginkan. pabila hal ini terjadi, maka dapat diperbaiki dengan cara menggunakan larutan silver oxide, Ag2O, dalam amonia berair juga disebut dengan reagen Tollens.
Karena atom hidrogen tidak terdapat pada keton, akan tetapi keton tetap tahan terhadap oksidasi, dan hanya zat pengoksidasi yang kuat seperti larutan kalium permanganat (VII) yang dapat mengoksidasi keton. akan tetapi, mereka melakukannya dengan cara yang berbeda, yaitu dengan cara merusak atau memutuskan ikatan karbon kemudian membentuk dua asam karboksilat.
1. Berdasarkan penjelasan diatas bahwa alkohol tersier merupakan alkohol yang tidak teroksidasi dalam suasana basa. Apabila jika dicoba mengoksidasi pada larutan asam maka alkohol tersier akan mengalami dehidrasi yang selanjutnya alkena akan teroksidasi. Mengapa hal tersebut bisa terjadi ?
2. Apakah kita bisa mengkondisikan suatu reaksi alkena dengan menggunakan kalium permanganat pada suasana panas namun tidak terjadi pemutusan ikatan?
3. Berdasarkan penjelasan diatas, maka dapat dipaparkan bahwa mekanisme reaksi oksidasi pada alkohol sekunder akan menghasilkan keton. Lalu bagaimana reaksi yang terjadi jika dioksidasi pada alkohol lainnya ?














Assamualaikum warahmatullahi wabarakatuh. Baiklah, saya Julia Krisnawati ingin mencoba menjawab permasalahan nomor 3. Jika direaksikan dengan alkohol lainnya maka produk yang dihasilkan juga akan berbeda. Produk yang dihasilkan ketika terjadi reaksi oksidasi pada alkohol primer adalah aldehid, yang jika direaksikan lebih lanjut akan menghasilkan asam karboksilat. Sedangkan pada alkohol tersier tidak terjadi reaksi oksidasi secara langsung. Menurut saya bisa saja terjadi, hanya saja harus diubah dahulu ke bentuk alkohol yang lain.
BalasHapusTerimakasih
Komentar ini telah dihapus oleh pengarang.
BalasHapusHallo Nestiya, saya Madalen Br. Pangaribuan NIM A1C119100 akan menjawab permasalahan nomor 1.
BalasHapusAlkohol tersier tidak dapat dioksidasi sebab tidak memiliki ikatan dengan antom Hidrogen(H). Karena tidak ada hidrogen yang bisa dilepaskan untuk bereaksi dengan oksigen maka tidak bisa terjadi reaksi oksidasi. Sekian dari saya semoga membantu terima kasih.